聚合物胶束递送平台
两亲性嵌段共聚物能够在水溶液中通过自组装形成聚合物胶束,其疏水嵌段构成胶束内核,可以有效包载疏水性药物;而亲水嵌段构成胶束外壳,有利于胶束的稳定和体内长循环。
子时纳米提供聚合物胶束定制服务,根据您所提供的需求以满足您理想的效果。

两亲性嵌段共聚物能够在水溶液中通过自组装形成聚合物胶束,其疏水嵌段构成胶束内核,可以有效包载疏水性药物;而亲水嵌段构成胶束外壳,有利于胶束的稳定和体内长循环。
1. 聚合物胶束组成材料
聚合物胶束由具有生物相容性的亲水链段和多功能载药核心的疏水链段组成。
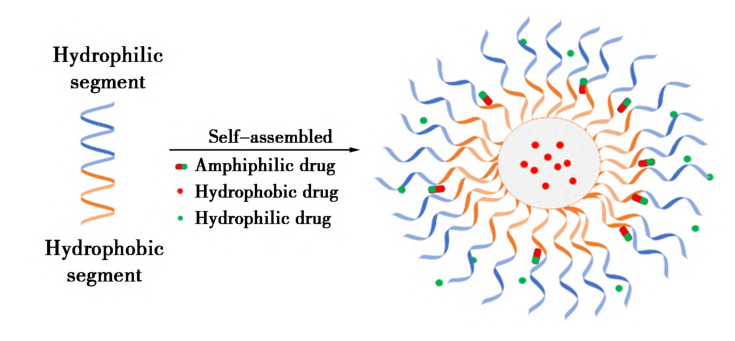
图1 水溶液中嵌段共聚物自组装成聚合物胶束
1.1 亲水链段材料
构成嵌段共聚物亲水链段的材料有聚乙二醇 (PEG)、聚乙烯醇(PVA)、聚〔N-(2-羟丙基)甲基丙烯酰胺〕 (PHPMA)、聚乙烯亚胺(PEI) 、聚 (N-异丙基丙烯酰胺) (PNIPAM)和聚乙烯吡咯烷酮(PVP)等。常用的亲水材料结构式如图2所示。PEG是目前使用最广泛的亲水链段材料。多柔比星 (doxorubicin , DOX)、喜树碱(camptothecin,CPT)和紫杉醇(pacli- taxel,PTX)等抗癌药物均已成功与PEG偶联。
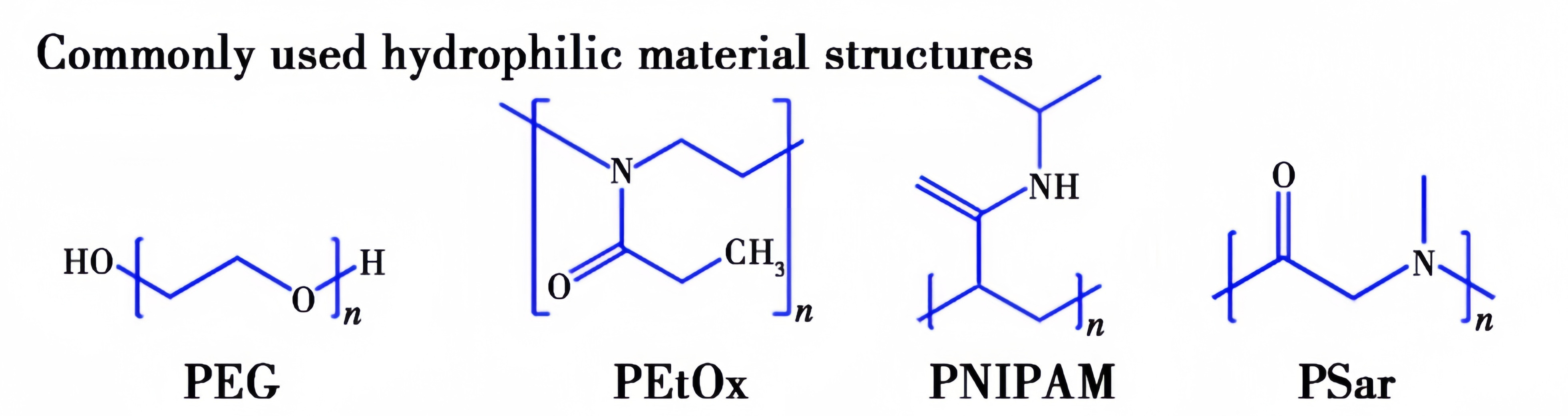
图2 常用的亲水材料结构式
Nosrat等制备了生物素功能化的聚乙二醇-聚己内酯(Biotin-PEG-PCL)胶束靶向递送青蒿素 (ar- temisinin,ART),以改善ART的不溶性。Biotin-PEG- PCL可以缓慢释放ART,促进其在体内循环。乳腺癌模型的体内抗癌活性表明,负载ART的胶束与对照组相比,肿瘤体积减小了40mm³,显著增加了肿瘤中药物的蓄积。
1.2 疏水链段材料
常用的合成材料有聚己内酯(PCL)、聚乙交酯(PGA)、聚丙交酯(PLA)、聚丙烯酸酯(PA)、聚苯乙烯(PS) 、聚乳酸-聚羟基乙酸共聚物 (PLGA)、精胺和短链磷脂等。常用疏水合成材料结构式如图3所示。
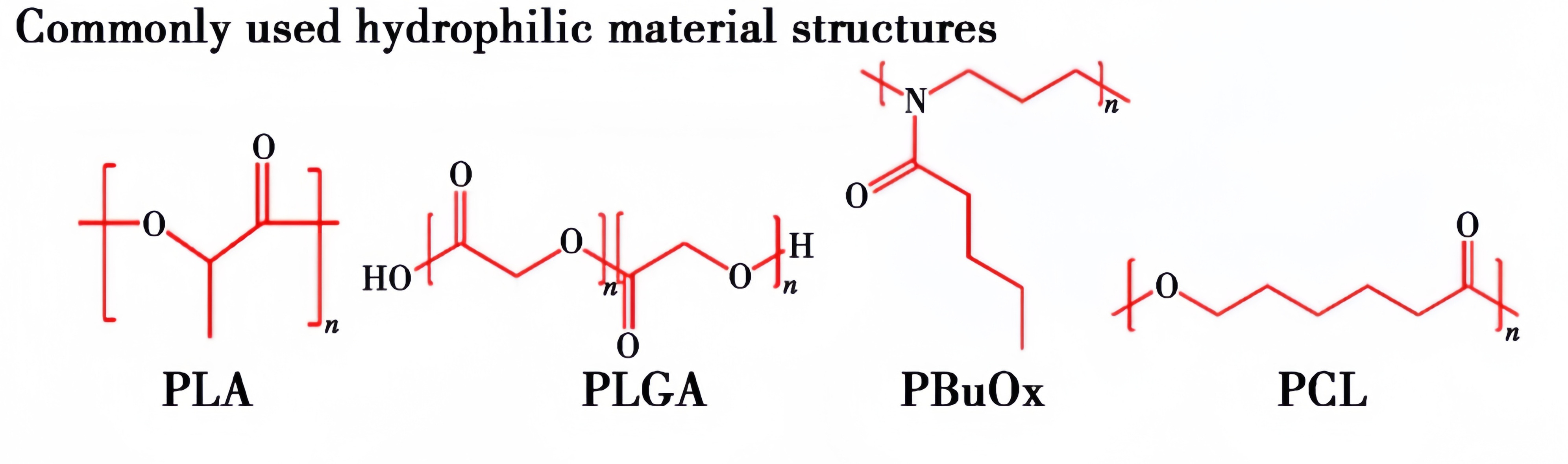
图3 常用疏水合成材料结构式
Chen等设计一种新型的壳聚糖衍生物(GACS-TPGS共聚物) ,以此构建聚合物胶束包载PTX。GA-CS-TPGS共聚物具有增强生物黏附、抑制P-糖蛋白(P-gp)外排和肝脏药物代谢等优点。胶束包载PTX后显著增强了药物的溶解性和通透性,提高了PTX的生物利用度和抗肿瘤效果。与Taxol®相比,该PTX胶束将PTX的生物利用度提高了约3.80倍,增强了PTX的抗肺癌效果。
2. 抗癌药物胶束制剂靶向策略
聚合物胶束因其良好的生物相容性、安全性和靶向性,已成为抗癌药物纳米递送系统的主流。聚合物胶束载体递送抗癌药物治疗肿瘤有被动靶向、主动靶向和刺激触发靶向3种策略。
2.1 主动靶向
主动靶向主要通过生物学的特殊相互作用将聚合物胶束与靶向配体结合。由于癌细胞和正常细胞的表面受体和抗原不同,靶向配体可识别癌细胞表面过度表达的靶点将癌细胞与正常细胞进行区分,将药物定向输送到肿瘤组织中,减少抗肿瘤药物对正常组织的不良影响,提高肿瘤组织中的药物浓度,改善细胞的识别能力,增强靶细胞的摄取能力,从而达到主动靶向的目的。目前叶酸、转铁蛋白、抗体和肽均已成功与聚合物胶束结合。
Kanazawa等开发了一种具有脑肿瘤靶向、经鼻入脑适用的聚合物胶束载体,该载体是由TAT肽和铃蟾素修饰的硬脂酰基共轭聚合物胶束(BOM/PEGPCL-TAT)包载CPT靶向递送。该胶束在脑瘤模型中展示出良好的脑部递送效果,显著提高了抗癌药物CPT的治疗效果。
2.2 被动靶向
被动靶向即自然靶向,是由于肿瘤组织周围血管内皮细胞之间的缺陷,导致聚合物胶束载体在肿瘤中的累积速率远高于正常组织;而淋巴系统的缺陷导致聚合物胶束滞留在肿瘤中,这种现象被称为实体瘤的高通透性和滞留效应(enhanced permeability and retention effect,EPR)。利用EPR效应药物胶束能被动靶向并滞留在癌症病变部位,以疗效好、副作用小的特点使药物达到治疗作用。
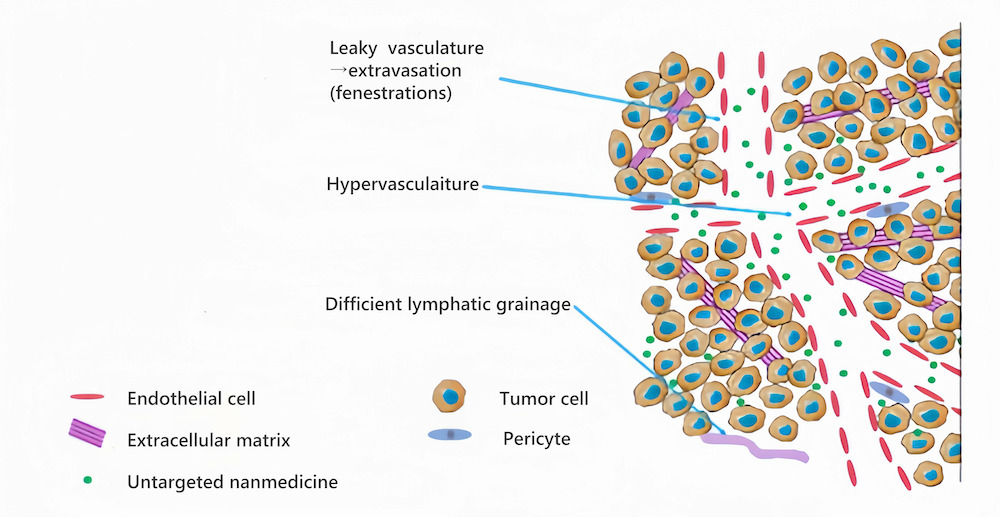
图4 常用疏水合成材料结构式
2.3 刺激触发靶向
刺激触发靶向即通过制备刺激敏感聚合物胶束,在各种物理、化学或生化来源的内源性刺激或外源性刺激下引发胶束的崩解、失稳、异构化、聚合或聚集的反应,从而导致药物的受控释放。在肿瘤环境中,内源性刺激包括低pH、氧化还原电位、炎症引起的高温以及各种过表达酶的存在;外源性刺激包括温度、光(紫外线、可见光和红外线)、磁场、电场和超声波。刺激敏感胶束通过在空间或时间上进行控制,实现对癌症实际治疗的按需控制,确保了抗癌胶束制剂靶向治疗的有效性和安全性。
Emami等研制了由α-生育酚(TOC)和肝素(HEP)组成的pH触发聚合物胶束,它可以包载多西紫杉醇(DTX)并靶向递送至乳腺肿瘤。负载DTX胶束具有pH药物释放依赖性。负载DTX胶束比游离DTX对乳腺癌细胞的毒性更大。与已上市的Taxotere®相比,负载DTX胶束治疗组的消除半衰期、血浆浓度曲线下面积和平均停留时间均显著增加。
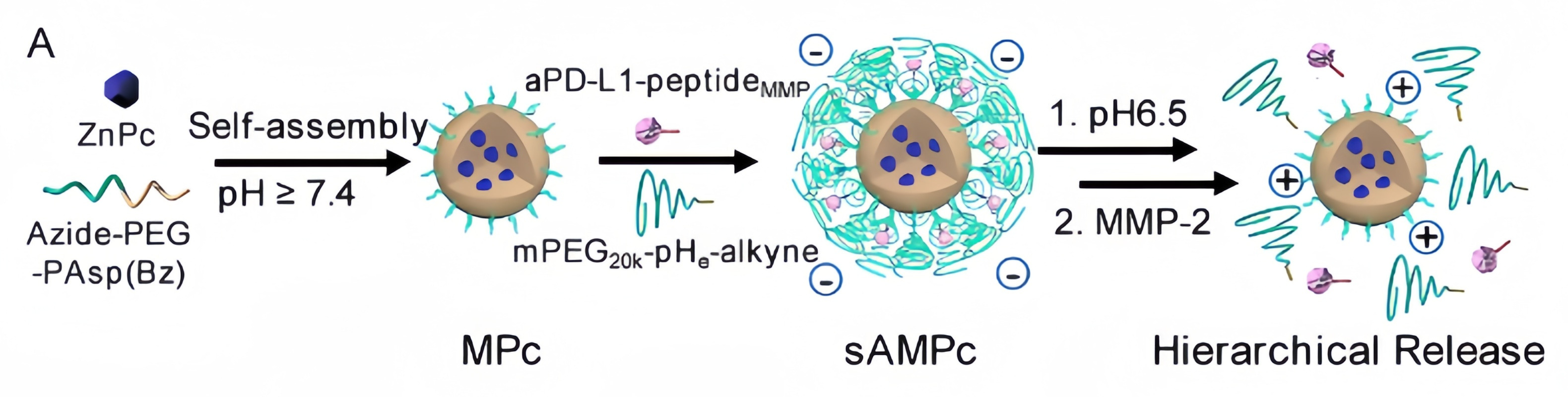
图5 常用疏水合成材料结构式
3. 抗癌药物共同递送胶束策略
针对癌症化学治疗机制的多样性,开发不同联合用药治疗方式以增加协同效应具有重大意义。目前聚合物胶束载体已被应用于抗癌药物联合用药、抗癌药物与基因共同递送、抗癌药物与光敏剂共同递送。
3.1 抗癌药物联合用药胶束制剂
由于不同抗癌药物之间具有协同作用、多药耐药逆转作用和靶向性,联合用药都表现出比相应的单一抗癌药物更好的治疗效果。聚合物胶束可以将两种或两种以上不同抗癌药物在有效剂量内按所需的比例进行包载,同时输送到同一肿瘤部位,以达到最好的协同效果。与单一载药系统相比,聚合物胶束能逆转多药耐药性,从而发挥更好的抗癌效果。
Wan等通过制备两亲性聚合物胶束包载PTX和顺铂(cisplatin,CDDP)用于联合治疗卵巢癌和乳腺癌。该胶束对两种药物的载药量超过50%,减缓了药物在血清中的释放,改善了药物代谢动力学,增加了药物在肿瘤中的分布。该研究表明共载PTX/ CDDP胶束的抗肿瘤活性优于单一药物胶束或其混合物。
3.2 抗癌药物与基因共同递送胶束制剂
克服耐药性的另一种方法是通过靶向沉默多药耐药相关蛋白〔如 P-gp、多药耐药蛋白1(MRP1)或抗凋亡蛋白(如 Bcl-2)〕基因,目前已开发出携带小干扰 RNA(siRNA)的聚合物胶束。与常规化学治疗的胶束制剂不同,聚合物胶束的表面可以通过修饰带正电荷,利用核酸带负电荷 的性质通过静电相互作用装载 siRNA,并且同时将疏水药物装载到疏水性内核中,同时实现化学治疗和基因治疗的协同治疗作用。
Christie 等通过嵌段共聚物与siRNA自组装,制备了粒径45 nm的稳定多功能聚乙二醇-聚(L-赖氨酸)(PEG-b-PLL)胶束。该胶束由2-亚氨基噻吩(2- IT)修饰的赖氨酸和PEG末端的精氨酸-甘氨酸-天冬氨酸环肽(cRGD)组成。将siRNA掺入含有cRGD的稳定胶束中,可以提高基因沉默和细胞摄取的能力,增加药物胶束在肿瘤组织和肿瘤相关血管中的蓄积。
3.3 抗癌药物与光敏剂共同递送胶束制剂
化学治疗和光疗的结合,对提高个性化精准治疗的安全性和有效性具有重大意义,在抗癌治疗中展示出良好的潜力。光疗指由非侵入性的光线刺激杀死肿瘤细胞,产生的副作用较小。光疗主要包括光动力疗法(photodynamic therapy,PDT)和光热疗法(photothermal therapy,PTT)两种形式,然而,由于光的穿透深度有限,单纯使用光疗很难将肿瘤完全消除,而化学治疗可以弥补这一缺陷。因此,将化学治疗与光疗进行联合的治疗方式将成为新一代癌症治疗的机遇和挑战。
Li等开发了活性氧(ROS)响应型聚合物胶束药物传递系统,以PTX前药和荧光光敏剂Cypate为疏水链段,以PEG为亲水链段包裹 PTX 形成聚合物胶束。Cypate是一种典型的近红外染料,同时用作光敏剂和光热剂,胶束包载后提高了溶解度,在近红外光照射条件下触发光疗,促进PTX渗透杀伤癌细胞,实现了两亲性聚合物胶束化学治疗与光疗的有机结合,展示了化学治疗与光疗联合治疗癌症的应用前景。
4. 抗癌药物胶束制剂产品研发进展
近几十年来,胶束制剂在癌症治疗中的作用尤为显著,在改善肿瘤药物治疗活性和减少药物毒性方面取得了巨大的成功,为抗癌药物纳米递送系统的进一步发展提供了坚实的基础。目前使用胶束制剂应用于临床研究的抗癌药物有 PTX、DOX、CDDP、7-乙基-10-羟基喜树(7-ethyl-10-hydroxycamptothecin,SN-38)等。
4.1 国外抗癌药物胶束制剂产品研发现状
4.1.1 国外临床抗癌药物胶束产品研究情况
NK012 是由化学偶联药物SN-38与PEGP(Glu)嵌段共聚物组成的胶束,主要用于治疗胃癌、直肠癌、乳腺癌 。SN-38是伊立替康盐酸盐(irinotecan hydrochloride,CPT-11)的生物活性代谢物,具有抗肿瘤活性,但由于其极差的溶解性限制了药物的市场潜力。NK012是有史以来第一个成功地以 20 nm的药物载体传递SN-38,载药量约为20%。NK012具有清除慢、肿瘤聚集率高的特点。在日本和美国分别进行了两项独立的Ⅰ期临床试验,研究发现NK102能显著抑制肿瘤活性。目前NK012处于Ⅱ期临床试验阶段。
NK105 是由 PEG-P(Asp)共聚物经 4-苯基-1-丁醇修饰的胶束,通过物理包埋法包裹PTX,适用于乳腺癌和胃癌的治疗。NK105的粒径约为85 nm,载药量约为23%,易溶于5%葡萄糖溶液,可静脉注射给药。NK105的PEG亲水外壳体积小、亲水性强,延长了药物的循环时间,显著降低了PTX的毒副作用。Nippon Kayaku公司于2004年开始NK105的Ⅰ期临床试验,目前在日本等地进行Ⅲ期临床研究。
NK911是载DOX的PEG-P(Asp)胶束,DOX以物理方式包埋在核中,粒径约为40 nm,适用于多种实体瘤。2001年在日本进入Ⅰ期临床试验,结果表明最低毒性剂量为67 mg/m2,推荐剂量为50 mg/m2。目前正在进行Ⅱ期临床研究。
NC-6004是负载CDDP的PEG-P(Glu)纳米胶束,载药量为39%,平均粒径为20 nm,主要用于胰腺癌的治疗。体外研究表明,该药物对各种癌细胞株的细胞毒性较低,体内抗肿瘤活性优于游离药物。NC-6004Ⅰ期临床研究于2006年在英国和美国启动,之后在中国和新加坡启动了针对晚期或转移性胰腺癌患者的Ⅰ/Ⅱ期临床研究。目前正在进行Ⅲ期临床研究。
SP1049C是由泊洛沙姆181(Pluronic L61)和泊洛沙姆 407(Pluronic F127)混合胶束组成负载DOX的新型配方,主要用于治疗多药耐药性肿瘤,已经通过了Ⅰ期和Ⅱ期临床试验,目前正在研究用于食管或胃食管交界处(gastroesophageal junction,GEJ)腺癌的Ⅲ期试验。研究结果表明Pluronic L61共聚物将仓鼠卵巢CHRC细胞的药物摄取率提高了7.2倍, 而Pluronic F127使该制剂具有物理化学稳定性,防止液相分离,并将胶束的有效尺寸保持在30 nm以下而不影响胶束体系的细胞毒性。部分国外临床研究的胶束制剂见表1。
4.1.2 国外上市抗癌药物胶束产品情况
Genexol®-PM是全球第一个上市的PTX聚合物胶束制剂,由mPEG-PLA共聚物自组装形成,平均粒径为 20~50 nm。Genexol®-PM原研公司为韩国Samyang,2007 年1月首次在韩国上市,现已在印度、菲律宾、越南、印度尼西亚等亚洲国家上市;作为一线药物主要用于治疗复发性或转移性乳腺癌、卵巢癌,并与CDDP 联合治疗非小细胞肺癌。Genexol®-PM在肿瘤中的生物分布显示PTX水平是Taxol®的2.0~3.0倍,其体内抗肿瘤效果明显优于Taxol®,另外研究表明Genexol®-PM使用安全,无过敏反应,大大降低了微生物污染和免疫抵抗的风险,具有更高的耐受剂量。
| 药物 | 药品名 | 聚合物结构 | 公司 | 临床试验 |
|---|---|---|---|---|
| SN-38 | NK012 | PEG-b-P(Glu-SN-38) | Nippon Kayaku(日本) | Ⅱ期 |
| PTX | NK105 | PEG-b-P(Asp-4-phenyl-1-butanol) | Nippon Kayaku(日本) | Ⅲ期 |
| DOX | NK911 | PEG-b-P(Asp-DOX) | Nippon Kayaku(日本) | Ⅱ期 |
| CDDP | NC-6004 | PEG-b-P(Glu) | Nano Carrier(日本) | Ⅲ期 |
| DOX | SP1049C | PluronicL6和Pluronic F127 | Supratek(加拿大) | Ⅲ期 |
Paclical®于2015年在俄罗斯获得批准上市,该胶束结构中引入了Oasmia Pharmaceutical公司独有的新型辅料XR-17。XR-17是一种可被机体代谢的维生素A类似物,可形成20~60 nm的胶束,对疏水药物PTX有增溶作用。研究结果表明,Paclical®与当前市场上销售的PTX制剂Taxol®(脂质体制剂)、Abraxane®(白蛋白结合制剂)与Genexol®-PM相比,其载药量大大提高。Nanoxel®的原研公司为Dabur Pharma,2007年在印度上市。Nanoxel®是以PVP-PNIPAM为载体制备的 PTX 聚合物胶束制剂,胶束粒径为 80~100 nm。Nanoxel®不含表面活性剂,主要用于转移性乳腺癌、卵巢癌、非小细胞肺癌及艾滋病相关Kaposi肉瘤的治疗。Nanoxel®与 Taxol®具有相同的药物代谢动力学特征和相似的抗肿瘤活性,但其不良反应较少,不会引起过敏反应,安全性有所提高。国外已上市的胶束制剂见表2。
| 药物 | 商品名 | 聚合物 | 公司 | 首次上市国家 | 上市年份 |
|---|---|---|---|---|---|
| PTX | Genexol®-PM | mPEG-PLA | Samyang (韩国) | 韩国 | 2007 |
| PTX | Paclical® | Micellar retinoid-derived | Oasmia Pharmaceutical (瑞典) | 俄罗斯 | 2015 |
| PTX | Nanoxel® | PVP-PNIPAM | Dabur Pharma (印度) | 印度 | 2007 |
4.2 国内抗癌药物胶束产品研发现状
根据国家药品监督管理局上市药品信息查询发现,目前国内仅有上海谊众药业股份有限公司产品注射用紫杉醇聚合物胶束获批上市(批准文号:国药H20210047).在药物临床试验登记与信息公示平台可以查询到国内处于临床试验的胶束制剂(表3)。
| 实验名称 | 相关药物 | 申报企业 | 临床试验 | 适应证 | 登记号 |
|---|---|---|---|---|---|
| 注射用紫杉醇聚合物胶束Ⅰ期临床研究 | 注射用紫杉醇聚合物胶束 | 丽珠集团丽珠医药研究所 | Ⅰ期 | 晚期实体瘤 | CTR20201313 |
| 注射用多西他赛聚合物胶束Ⅰ期临床研究 | 注射用多西他赛聚合物胶束 | 广东众生药业股份有限公司 | Ⅰ期 | 晚期实体瘤 | CTR20200464 |
| 多西他赛聚合物胶束在晚期恶性实体瘤患者的I期临床研究 | 注射用多西他赛聚合物胶束 | 苏州海特比奥生物技术有限公司 | Ⅰ期 | 恶性实体瘤 | CTR20192730 |
| 多西他赛聚合物胶束治疗复发转移性乳腺癌Ⅰ期临床研究 | 注射用多西他赛聚合物胶束 | 山东华铂凯盛生物科技有限公司 | Ⅰ期 | HER2阴性的复发转移性乳腺癌 | CTR20190525 |
| 注射用紫杉醇聚合物胶束对比紫杉醇注射液的有效性研究 | 注射用紫杉醇聚合物胶束 | 深圳市天翼药物技术有限公司/ 南京泛太化工医药研究所 | Ⅱ期 | HER2阴性复发或转移性乳腺癌 | CTR20150197 |
| 注射用紫杉醇聚合物胶束的安全性和有效性研究 | 注射用紫杉醇聚合物胶束 | 深圳市天翼药物技术有限公司/ 南京泛太化工医药研究所 | Ⅰ期 | 恶性肿瘤 | CTR20150196 |
文章信息源于文献:《聚合物胶束作为抗癌药物纳米递送载体的研究进展》,登载该文章目的为更广泛的传递行业信息,不代表赞同其观点或其真实性负责。文章版权归原作者及原出处所有,文章内容仅供参考。本网拥有对此声明的最终解释权,若侵犯版权,请联系小编删除

